Czym są nowotwory jelita grubego?
Nowotwór jelita grubego jest to nowotwór występujący w obrębie okrężnicy, zgięcia esiczo-odbytniczego i odbytnicy.
Rak jelita grubego rozwija się w większości przypadków na podłożu uszypułowanego, znacznie rzadziej nieuszypułowanego gruczolaka, w którym poprzez procesy metaplastyczne doszło do powstania raka nieinwazyjnego (tzw. raka in situ, CIS) – obecnego wyłącznie w obrębie błony śluzowej, a następnie inwazyjnego (po nacieczeniu poza blaszkę właściwą błony śluzowej).
W 90-95% przypadków zachorowanie na nowotwór złośliwy jelita grubego jest sporadyczne, w pozostałych 5-10% występuje podłoże dziedziczne.
U chorych na raka jelita grubego, nawet jeśli wiemy, na jakie czynniki byli oni narażeni, trudno jest określić, który z nich odegrał kluczową rolę w rozwoju raka.
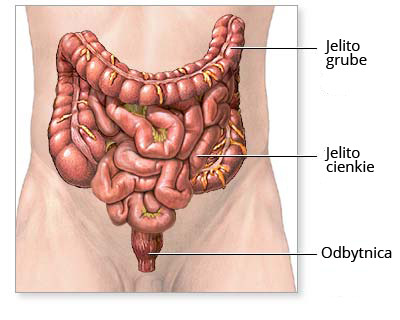
Ryc. Schemat anatomiczny jelit